一、背景介紹
本試劑盒是用來定量分析以大腸桿菌(E.coli)為表達系統(tǒng)時,蛋白藥物中宿主細胞殘留蛋白。
大腸桿菌被廣泛用來作為表達系統(tǒng),在破碎菌體提取目標蛋白過程中,很大一部分宿主蛋白與目的蛋白一起釋放,該宿主蛋白具有很強的免疫原性,導致不良的毒性或免疫反應而危及產品安全和質量,造成潛在的生物污染,生物醫(yī)藥產品生產下游過程的目的之一就是移除這些潛在危害。
因此,非常有必要將宿主細胞蛋白(HCP)殘留量降低到最低水平,在研發(fā)下游純化的工藝時,必須具有一種科學合理的測定成品或者半成品中HCP濃度的方法,而酶聯(lián)免疫法具有極高靈敏度,因而被FDA,EMA,NMPA及ICH等國內外監(jiān)管機構定為HCP檢測的金標準。
二、實驗原理
本試劑盒采用了固相夾心法的酶聯(lián)免疫吸附實驗(ELISA)。先將捕獲抗體包被微孔板,制成固相抗體。檢測時在包被抗體的微孔板中先加入待測抗原孵育,洗滌后加入辣根過氧化物酶(HRP)標記的檢測抗體,形成包被抗體-抗原-檢測抗體復合物。經洗滌后去除未參與反應的結合物,最后加入底物TMB顯色。TMB在HRP的氧化作用下轉化成藍色,并在酸的作用下轉化成最終的黃色。氧化后的TMB顏色和因子的總含量呈正相關。用酶標儀在450nm波長下測定吸光度(OD值),與濃度擬合成標準曲線,通過樣本OD值,代入標準曲線方程,計算樣品中因子濃度。
三、試劑盒優(yōu)勢
1. 覆蓋度廣:抗體有較強的識別HCP能力,覆蓋度80%以上,工藝穩(wěn)定。
2. 抗體滴度高:試劑盒中使用的抗體,間接法Elisa檢測抗血清效價達106。
3. 靈敏度高:血清抗體純化采用親和純化,最大限度去除非特異性抗體。
4. 穩(wěn)定性高:生產過程采用廣譜蛋白穩(wěn)定劑,和微孔板處理工藝,增加標準品及微孔板熱穩(wěn)定性和結果的可重復性。
5. 適用性:試劑盒適經不同反應溫度(20-30度)和不同反應時間(±10分鐘)測試,檢測結果重現性較好。
6. 稀釋液優(yōu)化:使用優(yōu)化稀釋液,可降低樣本檢測過程中非特異性吸附,本底顯色極低利于觀察待測樣本濃度。
四、試劑盒組分
名稱 | 規(guī)格 | 數量 | 保存 | |
1 | 已包被平底微孔板 | 96孔 | 1板(可拆卸) | 2-8℃密封冷藏 |
2 | 標準品母液(500μg/mL) | 50μL | 1管 | 2-8℃冷藏 |
3 | 檢測抗體母液(100×) | 150μL | 1管 | 2-8℃冷藏 |
4 | TMB | 10mL | 1瓶 | 2-8℃避光冷藏 |
5 | 終止液 | 10mL | 1瓶 | 2-8℃冷藏 |
6 | 洗液(20×) | 10mL | 5瓶 | 2-8℃冷藏 |
稀釋液(10×) | 10mL | 1瓶 | 2-8℃冷藏 | |
8 | 封板膜 | 4張 | ||
使用說明書 | 1份 |
五、實驗需要但未提供的耗材及設備
1. | 移液器:10μL-1000μL | 6. | 酶標儀 |
2. | 多道移液器 | 7. | 高速離心機 |
3. | 滅菌的去離子水或超純水1L | 8. | 迷你離心機 |
4. | 滅菌EP管 | 9. | 洗板機或者洗瓶 |
5. | 吸水紙 | 10. | 數據分析及繪圖軟件 |
六、實驗前的準備
請仔細閱讀試劑盒說明書,反應在室溫(20-25度,下同)下進行。
七、試劑的準備
1. 試劑盒內所有試劑及包被板,請在使用前30分鐘拿出,使其恢復室溫。
2. 洗液的稀釋:將5瓶體積為10mL的20×洗液母液,加入950mL去離子水或超純水,混勻備用。如果濃縮液中有少許結晶,請將其置于室溫,并輕輕震蕩至晶體完全溶解。
3. 稀釋液的準備:將10mL 10×稀釋液母液,加入90mL去離子水或超純水,混勻備用。如果濃縮液中有少許結晶,請將其置于室溫,并輕輕震蕩至晶體完全溶解,用作標準品,樣品,檢測抗體的稀釋液。
八、操作步驟
1. 撕開包裝袋,取出包被有抗體的酶標板,拆下不需要使用的板條,并用封板膜封好,放回鋁箔袋,重新放回4℃保存(板架可重復使用)。標準品由于運輸顛簸可能會粘在管壁上,使用前輕微甩勻,或在離心機上離心2秒左右。
2. 標準品的稀釋:
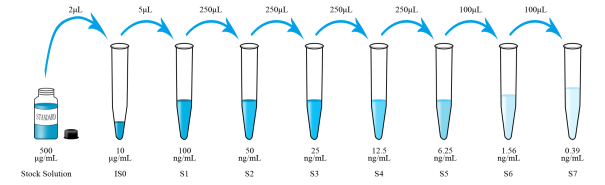
配置標曲時提前標記8只樣品稀釋管,預加入一定體積的稀釋液,其中IS0(98μL),S1(495μL),S2至S5(各250μL),S6-S7(各300μL)。
(1)取2μL標準品母液(濃度為500μg/mL)加入到標記為IS0的管,輕輕吹打2次并顛倒混勻(后續(xù)操作相同,切勿渦旋等劇烈混勻)。
(2)取5μL濃度為10μg/mL的IS0到S1管,輕輕吹打2次并顛倒混勻。
(3)取250μL濃度為100ng/mL的標準品S1到S2,之后以2倍梯度稀釋至S5。
(4)取100μL濃度為6.25ng/mL的S5至S6中(4倍稀釋),輕輕吹打2次并顛倒混勻。
(5)取100μL濃度為1.56ng/mL的S6至S7中(4倍稀釋),輕輕吹打2次并顛倒混勻。
注:標準曲線有7個點,分別命名為S1、S2、S3……S7。其中S1即標準曲線的最高濃度點(100ng/mL)。
3. 加樣:取100μL標準品及待測樣本加入微孔板中。空白對照(Blank Control)加入100μL樣本稀釋液即可。
4. 將酶標板用封板膜密封后室溫振蕩孵育1.5小時。
5. 洗板機洗板:
? 取出稀釋好的洗液放置于洗板機的洗瓶中備用。
? 取出上步中的微孔,甩去微孔中的液體,洗板機洗板5次。
? 洗板完成后,將微孔板倒扣在吸水紙上拍打,充分拍干至無明顯水膜為止。
或手動洗板:
? 取出稀釋好的洗液放置于洗瓶中備用。
? 取出上步中的微孔,甩掉微孔中的液體,在吸水紙上輕輕拍打至無明顯液滴。
? 用多道移液槍向每個微孔中加300μL洗液,靜置20秒,倒去洗液,將微孔板倒扣在吸水紙上輕輕拍打。重復5次。注:第五次洗板時,充分拍干至無明顯水膜為止。
6. 檢測抗體:取檢測抗體母液(100×)100μL到9.9mL稀釋液中稀釋至工作濃度(1×),取100μL加入到各微孔中,將酶標板用封板膜密封后室溫振蕩孵育1.5小時。
7. 洗板:重復步驟5。
8. 顯色:各微孔板加入100μL TMB溶液,室溫反應15分鐘左右。若顏色淺可適當延長反應時間,勿超過30分鐘。
9. 終止:各微孔中加入50μL終止液,終止反應。
10. 讀取OD值:在波長450nm下讀取OD值。
11. 數據分析:推薦使用四參數回歸擬合。
九、注意事項
(一)樣本收集注意事項
1. 樣本收集完畢后,要分裝保存在-20℃(少于3個月)或-80℃(少于6個月)以保持蛋白活性,避免污染和反復凍融。如果要在24小時內分析樣本,可以保存在2-8℃。
2. 冷凍樣本使用前請保證充分化凍(請勿加熱融化樣本),使用前用移液器或者Vortex混勻,樣本液中含有沉淀物會對ELISA有干擾,可離心去除。
3. 某些化學裂解液(如SDS,Triton等)可能會對本實驗造成干擾,謹慎使用。
4. 建議所有標準品及樣本都設置復孔。向微孔中加入樣本,保證不要有氣泡。
5. 目標蛋白純化過程通常伴隨成分復雜的緩沖液,建議首次使用不同緩沖液時進行加標回收,以排除基質干擾效應。通常,高鹽、低pH、多糖、有機溶劑及去污劑會導致較低回收率。具體做法:將稀釋后的標準品S1(100ng/mL)與待測試溶液基質按照1:1體積混合(如50μL含/不含濃度為100ng/mL的標準品S1加入50μL待測溶液),計算時用加標后濃度減去加標前本底濃度,再除以理論濃度即為加標回收率。
(二)實驗操作注意事項
1. 請不要將本試劑盒的試劑與其他試劑盒試劑交叉使用。
2. 實驗操作使用一次性吸頭,避免交叉污染。
3. 加樣:加樣時要控制時間和速度,一般加樣時間控制在10分鐘內。如果樣本數量過多,可使用多道移液器。
4. 洗滌:洗滌時微孔中殘留的洗滌液應在吸水紙上充分拍干,并要消除板底殘留的液體和手指痕跡,避免影響最后的酶標儀讀數。
5. 由于底物TMB溶液是光感性的試劑,使用前請勿長時間暴露于可見光下。同時要避免TMB與金屬接觸。
6. 反應時間的控制:加入底物后請定時觀察反應孔的顏色變化(比如,10分鐘左右),如果顏色較深,請?zhí)崆凹尤虢K止液終止反應。
7. 本試劑盒中使用了稀硫酸作為終止液,其具有輕微腐蝕性,使用時應避免接觸衣物或眼、手等皮膚暴露部位。
8. 標準曲線的R2≥0.95。
9. 拍板示意圖:
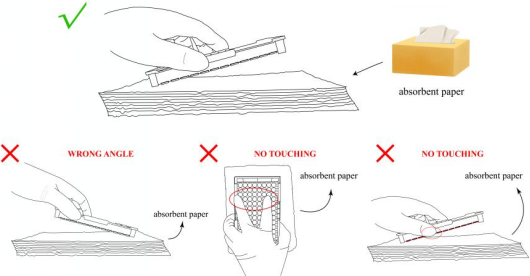
十、數據處理
1. 對樣本及標準品各自對應的復孔OD值取平均值。
2. 以標準品的OD作為Y值,標準品的濃度作為X值,推薦選擇四參數logistic(4-PL)曲線擬合。
3. 將樣本OD代入到標準曲線方程中計算樣本中待檢樣本的濃度。
4. 以下曲線僅供參考。
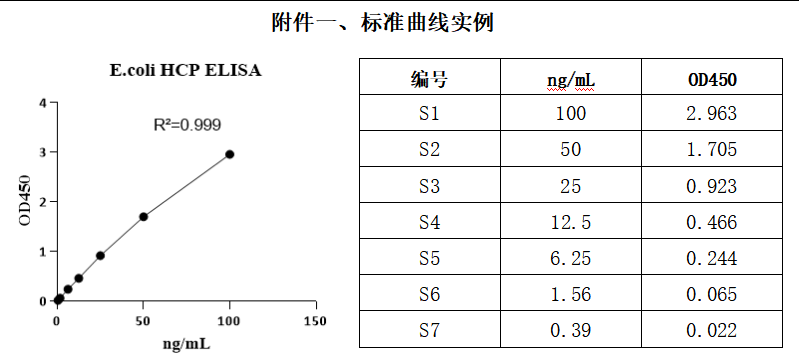
十一、試劑盒質量控制
1. 靈敏度
最低檢測限(LOD):0.195ng/mL 最低定量限(LOQ):0.39ng/mL
2. 精密度
批內差CV%: 7.3-13.1 批間差CV%:8.1-11.5
3. 特異性
樣品 | 濃度 |
HEK293 HCP | Not Detectable |
CHO HCP | Not Detectable |
畢赤酵母HCP | Not Detectable |
漢遜酵母HCP | Not Detectable |
釀酒酵母HCP | Not Detectable |
十二、常見問題及分析
若實驗結果顯示異常,請及時對顯色結果進行拍照記錄,并完整保存未使用的板條及試劑,同時聯(lián)系技術支持。此外,亦可參考后續(xù)提供的排查信息以確定問題根源。
問題描述 | 可能原因 | 相應對策 |
標準曲線 梯度差 | 稀釋錯誤 | 按照相應比例稀釋標準曲線 |
吸液或加液不準 | 檢查移液器及吸頭 | |
酶標板洗滌不完全 | 保證洗板次數及每孔的洗液用量 | |
顯色很弱或無色 | 溫育時間太短 | 保證足夠的溫育時間 |
實驗溫度不正確 | 使用推薦的溫育溫度 | |
試劑體積不夠或漏加 | 檢查吸液及加液過程,保證所有試劑按順序足量添加 | |
顯色液沒有恢復室溫 | 顯色前將TMB放置室溫半小時以上 | |
OD值讀數低 | 酶標儀設置不正確 | 在酶標儀上檢查波長和濾光片裝置 |
讀數前應提前打開酶標儀進行預熱 | ||
變異系數(CV值)大 | 加液不正確 | 檢查加液情況 |
酶標板底部有污染 | 檢查酶標板底部是否有殘留的液體和手印 | |
板孔內有異物或氣泡 | 加樣前確認板孔內無異物,加樣后確認無氣泡 | |
溫育過程中未封板或封板不完全 | 用封板膜封板 | |
背景值高 | 酶標板洗滌不完全 | 按說明書推薦的方法進行洗板 |
如果用自動洗板機,請檢查所有的加液口和排廢液口是否有堵塞 | ||
如果是手洗板,可適當增加洗板次數 | ||
洗滌不充分漏洗都會導致高背景 | ||
溫育時間、溫度不正確 | 按照說明書嚴格要求操作 | |
耗材污染 | 使用的管子、槍頭等耗材不干凈 | |
洗液有污染 | 配制新鮮洗液 | |
顯色液被污染 | 顯色溶液自身是沒有顏色的,確保底物在使用之前沒有被金屬離子或氧化試劑污染,而且避光保存 | |
靈敏度低 | 試劑盒保存不當 | 按說明書要求保存相關試劑 |
應用:定量檢測蛋白純化過程及終產物中宿主細胞蛋白殘留
用途:本試劑盒僅供科研和生產使用,不得用于臨床及診斷!
你可能感興趣
評價 (0)
留言板

